|

|
Suivi post-thérapeutique : nouvelles recommandations
 Xavier CARCOPINO |
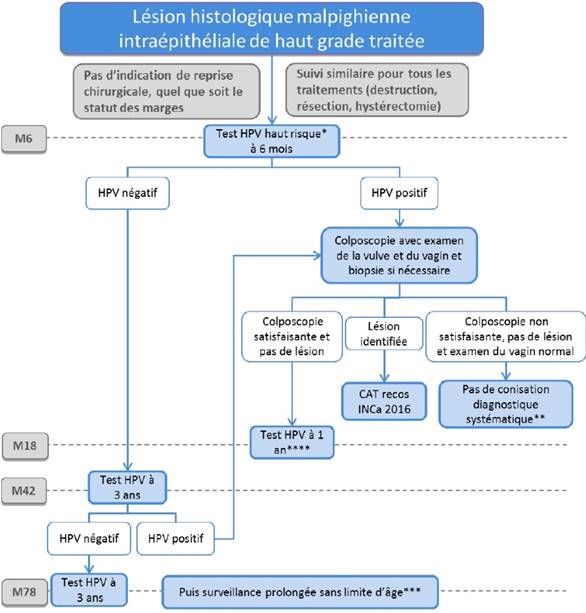
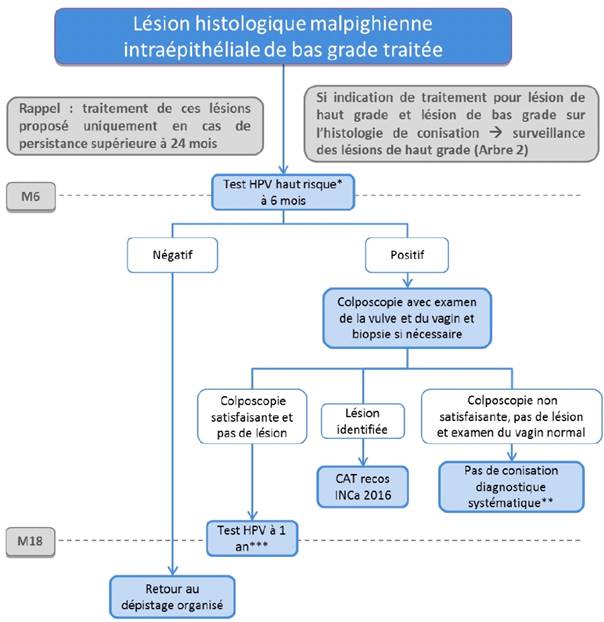
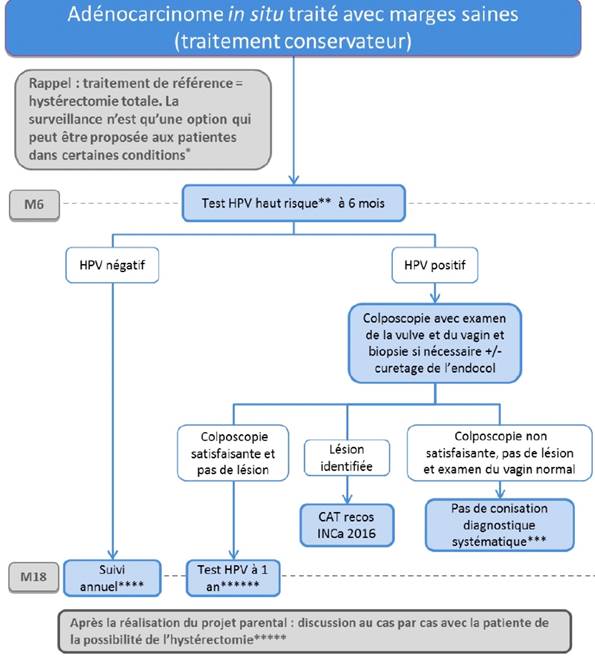
Si le traitement des lésions intraépithéliales de haut grade du col de l’utérus est extrêmement efficace et permet d’éviter l’évolution vers un cancer, il faut garder à l’esprit que ces patientes ne peuvent plus être considérées comme relevant du dépistage. En effet, le risque de récidive impose la mise en place d’une surveillance spécifique adaptée et prolongée. Ce risque est globalement estimé à près de 15 %.1 Et s’il est maximal lors des deux premières années suivant le traitement, il persiste pendant de nombreuses années. En plus du risque de récidive d’une lésion intra-épithéliale, ces patientes sont également exposées à un risque de développer un cancer du col utérin 4 à 5 fois plus important que celui de la population générale.2–4 On notera que ce risque persiste plus de 10 ans après le traitement initial et probablement tout au long de la vie de la patiente. Un suivi adapté et prolongé des patientes ayant été traitées pour une lésion intraépithéliale du col utérin est donc nécessaire. Reste à identifier les outils les plus performants pour suivre ces patientes, permettre d’identifier les récidives éventuelles et éviter l’apparition d’un cancer. Si les marges de résection sont statistiquement associées au risque de récidive, elles ne sont pas en pratiques suffisamment prédictives de ce risque et aucune décision ne peut donc être prise sur ce seul paramètre. Si l’obtention de marges non saines multiplie par 5 le risque de récidive, celui-ci reste faible, de l’ordre de 17 % contre 4 % pour des marges saines.5 Ainsi, en l’absence de micro-invasion, la présence de marges non saines sur l’analyse histologique de la pièce de résection ne doit pas faire indiquer une reprise chirurgicale immédiate.6 Celle-ci est le plus souvent inutile avec l’absence de lésion résiduelle dans plus de 80 % des cas et surtout augmente le risque de colposcopie insatisfaisante par sténose cicatricielle de l’orifice cervical et/ou jonction de type 3. Il est donc recommandé de n’indiquer un nouveau traitement que si la surveillance post-thérapeutique met en évidence une récidive. Le suivi post-thérapeutique reposait jusqu’ici sur la pratique combinée du frottis et de la colposcopie à 6 mois puis à un an avec un frottis annuel lorsque ces examens étaient normaux. Si cette modalité de surveillance est efficace, elle souffre néanmoins d’une spécificité imparfaite à l’origine de nombreuses « fausses alarmes ». En effet, les processus cicatriciels initiés par les traitements réalisés sont à l’origine de perturbations du frottis mais également de la colposcopie. Ces perturbations sont à l’origine d’une augmentation du nombre de biopsies réalisées et donc du risque de nouveau traitement injustifié.7 Les données actuelles de la littérature médicale ont clairement démontré la supériorité du test HPV sur toutes les autres modalités du suivi post-thérapeutique.8 Le test HPV est plus sensible que le frottis pour la détection des récidives post-traitement des lésions intraépithéliales du col de l’utérus et a une spécificité équivalente. Mais son principal atout est son extraordinaire valeur prédictive négative. Cela signifie qu’un test HPV négatif après le traitement d’une lésion intraépithéliale permet d’éliminer une récidive et une lésion résiduelle. Le test HPV est donc le test de choix pour valider le succès thérapeutique après le traitement d’une lésion intra-épithéliale du col utérin. De plus, la durée de la protection donnée par un test HPV négatif est prolongée, estimée à au moins 3 ans et pouvant aller jusqu’à 5 ou 6 ans selon les études.9 Cela permet d’espacer l’intervalle de temps entre les tests de suivi post-thérapeutique. Le principal défaut du test HPV est que près de 30 % des patientes restent HPV positives après le traitement d’une lésion intraépithéliale de haut grade.10 Mais si un test HPV négatif signifie absence de lésion et succès thérapeutique, un test HPV positif ne veut pas dire qu’il y a une lésion mais qu’une colposcopie est nécessaire. En pratique, la probabilité de lésion intraépithéliale de haut grade chez une patiente ayant un test HPV positif en post-traitement n’est que de 20 % environ.10 L’INCa vient de publier de nouvelles recommandations pour le suivi post-thérapeutique des lésions intraépithéliales du col utérin.11 Schématiquement, le test HPV est désormais le test de suivi recommandé en première intention et doit être réalisé 6 mois après le traitement. Le frottis n’a plus sa place dans le suivi de ces patientes et la colposcopie n’est indiquée que pour les femmes ayant un test HPV positif. Suivi après le traitement d’une lésion intraépithéliale de haut grade du col utérin(Figure 1) Le suivi doit être le même quelle que soit la méthode thérapeutique utilisée. Il n’y a pas d’indication de reprise chirurgicale chez les femmes ayant des marges non saines. Un test HPV est indiqué 6 mois après le traitement. Il n’y a pas d’indication à réaliser un test de génotypage. Si le test est négatif, les patientes auront un test HPV trois ans plus tard et tous les 3 ans tant qu’il reste négatif. Etant donné le risque prolongé de récidive et de cancer, le suivi de ces patientes devra être prolongé, sans limite d’âge. Une colposcopie avec examen du vagin et de la vulve et biopsie si nécessaire devra être réalisée si le test HPV est positif. Les patientes dont la colposcopie est satisfaisante et ne retrouve pas de lésion devront avoir un test HPV de contrôle un an plus tard. Dans le cas où une lésion est identifiée, celle-ci devra être prise en charge selon les recommandations actuelles. Enfin, si la colposcopie n’est pas satisfaisante, il n’y a pas d’indication de conisation diagnostique systématique. Les outils existants (frottis, curetage de l’endocol, test HPV, colposcopie…) pourront être utilisés pour décider de la prise en charge. On notera que ces recommandations s’appliquent également aux patientes ayant eu une hystérectomie et ayant un antécédent de lésion intra-épithéliale de haut grade du col utérin. Ceci est justifié par le risque de récidive vaginale et de cancer du vagin imposant la surveillance de celui-ci. Suivi après le traitement d’une lésion intraépithéliale de bas grade (Figure 2) On distingue deux situations différentes pour le suivi post-thérapeutique des lésions de bas grade. Pour les patientes ayant eu une lésion de bas grade diagnostiquée puis traitée (après au moins deux ans de surveillance selon les recommandations actuelles), un test HPV sera réalisé 6 mois après le traitement et la patiente pourra retourner dans le dépistage si ce test est négatif. Une colposcopie ne sera indiquée que si le test HPV est positif. Par contre, les patientes chez lesquelles une lésion de bas grade a été mise en évidence sur l’analyse d’une pièce de conisation indiquée pour le traitement d’une lésion intra-épithéliale de haut grade documentée par une biopsie préalable devront bénéficier du même suivi que les patientes traitées pour une lésion de haut grade. Suivi après le traitement d’un adénocarcinome in situ (Figure 3) Rappelons que le traitement de ces patientes repose sur l’hystérectomie qui devra être réalisée après une conisation en marges saines. Un traitement conservateur peut être réalisé pour les femmes ayant un projet de grossesse, ayant eu une conisation en marges saines, ayant été informées du risque de récidive, souhaitant une surveillance et acceptant les principes de la surveillance. Dans tous les cas, le suivi sera le même que celui d’une lésion intra-épithéliale de haut grade avec un test HPV à 6 mois puis tous les 3 ans s’il est négatif avec une Figure 1. Recommandations pour la surveillance post-thérapeutique des lésions intra-épithéliales de haut grade du col utérin. Figure 2. Recommandations pour la surveillance post-thérapeutique des lésions intra-épithéliales de bas grade du col utérin. Figure 3. Recommandations pour la surveillance post-thérapeutique des adénocarcinomes in-situ du col utérin. Références bibliographiques :
1. Kocken M, Helmerhorst TJM, Berkhof J, Louwers JA, Nobbenhuis MAE, Bais AG, et al. Risk of recurrent high-grade cervical intraepithelial neoplasia after successful treatment: a long-term multi-cohort study. Lancet Oncol. 2011 May;12(5):441–50. 2. Soutter WP, de Barros Lopes A, Fletcher A, Monaghan JM, Duncan ID, Paraskevaidis E, et al. Invasive cervical cancer after conservative therapy for cervical intraepithelial neoplasia. Lancet Lond Engl. 1997 Apr 5;349(9057):978–80.
|